Indicaciones de la cirugía de cataratas en niños
Las cataratas congénitas pueden causar discapacidad visual en los niños[1]. Es la causa de aproximadamente 10% de los casos de ceguera infantil en todo el mundo.[2]. En particular, una proporción significativa de casos se produce en los países en desarrollo[3,4].
Debido al rápido desarrollo de la visión en los primeros 4 meses de vida (desarrollo del reflejo de fijación), una falta o limitación de las sensaciones visuales debida a una lente opaca conduce en la mayoría de los casos a ambliopía, estrabismo, nistagmo o incluso a una disminución secundaria de las neuronas de los cuerpos geniculados laterales y del córtex visual (SDV - Síndrome de Privación Visual).
Las causas de las cataratas congénitas son innumerables; cabe destacar los factores genéticos, las infecciones intrauterinas, el uso de fármacos durante el embarazo y los trastornos metabólicos infantiles.[1]. El tratamiento clínico depende principalmente de la naturaleza y la gravedad de la catarata. La ambliopía, las dificultades intra y postoperatorias y las frecuentes revisiones médicas convierten el tratamiento de las cataratas congénitas en un reto importante.
Todas estas cuestiones hacen que la cirugía de cataratas en niños sea técnicamente más compleja que en adultos.
Indicaciones de la cirugía de cataratas en niños
La principal indicación para la extracción de cataratas es la opacificación del cristalino, que impide el desarrollo visual normal.
¿Cuándo operar las cataratas en los niños?
En general, se admite que la mayor disminución de la agudeza visual se produce en las primeras semanas de vida. Hasta las 14 semanas de edad, cada retraso de tres semanas provoca una disminución de la agudeza visual de una línea en las tablas de Snellen. Entre las 14 y las 31 semanas de edad se produce una ligera disminución adicional de la agudeza visual. La cirugía de cataratas realizada antes de las 4 semanas de edad reduce la incidencia de estrabismo y nistagmo.[5].
Se considera que las cataratas unilaterales deben operarse antes de la sexta a octava semana, y las bilaterales antes de la décima semana de edad[6,7]. Debido al riesgo de ambliopía, el tratamiento quirúrgico debe realizarse lo antes posible. Sin embargo, en la bibliografía se señala una mayor incidencia de glaucoma secundario si el tratamiento quirúrgico se realiza demasiado pronto.[5,7,8].
Biometría y cálculo de la potencia de la lente intraocular
El importante crecimiento del ojo en los primeros años de vida del niño y las dificultades para predecir la longitud final del globo ocular son la causa principal de los problemas para calcular la potencia de las lentes intraoculares. Los cambios refractivos son el resultado del aumento de la longitud axial del globo ocular, que varía de 16,8 mm en el lactante a 22,6 mm en el adulto, y del cambio en la curvatura de la córnea (51,2 D en el lactante; 43,5 D en el adulto) y del cristalino (34,4 D en el lactante; 18,8 D en el adulto).
Esto hace que la mayoría de los cirujanos prefieran hipocorregir a los niños pequeños en el momento de la cirugía (buscando una corrección hipermetrópica), en previsión de un cambio miópico significativo con el tiempo. Enyedi et al propusieron directrices para identificar los objetivos refractivos a diferentes edades basándose en los datos de su estudio, como se muestra en la Tabla I[9].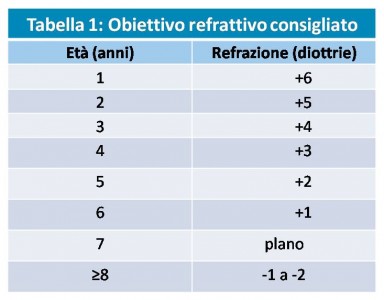
Basándose en los datos de varios estudios, no se ha puesto de manifiesto que una de las fórmulas utilizadas en el cálculo de la potencia de la lente intraocular sea más eficaz. Normalmente se aplican SRK II, SRK/T, Hoffer Q y Holladay.[10]. Dahan et al sugieren dejar un 20% en menores de dos años y un 10% en niños de 2 a 8 años.[11]. Lu et al reducen la potencia de implantar un 30% en niños de 6 a 12 meses. Después de la cirugía, todos los niños deben ser corregidos con gafas o lentes de contacto.[12].
Elección de una lente intraocular (LIO)
La elección de la LIO y la edad del niño en el momento de la implantación son objeto de controversia.
Hay que recordar que cuanto más joven es el paciente en el momento de la implantación de la LIO, mayor es el riesgo de reintervención debido a complicaciones[13]. Las lentes intraoculares artificiales suelen implantarse en niños mayores de 2 años (en el primer año de vida la refracción cambia en torno a 10 D).
En la literatura actualmente disponible, la edad mínima de los pacientes quirúrgicos para la implantación de LIO es de 7 días[14]. LU et al afirman que los implantes de lentes intraoculares son seguros en niños de entre 6 y 12 meses de edad[12].
El lugar más utilizado para la implantación de la LIO es el saco capsular. Garantiza el secuestro de la LIO del tejido vascularizado. La fijación de la LIO en el surco ciliar crea más problemas, ya que la lente entra en contacto con la coroides. Algunos oftalmólogos pediátricos afirman que la inserción de la lente intraocular en el saco para los ojos afáquicos es ideal, pero se trata de una técnica muy difícil[15].
Observaciones previas han mostrado muy buenos resultados con la implantación de lentes acrílicas hidrofílicas[3,16]. La AAPOS (Asociación Americana de Oftalmología Pediátrica y Estrabismo) recomienda la lente AcrySoft de una pieza para su implantación en niños. Es fácil de implantar y es segura incluso en lactantes y niños con macroftalmia. La implantación de lentes acrílicas hidrofóbicas se asocia a un menor riesgo de opacificación de la cápsula posterior y glaucoma secundario.[3]. Se observaron depósitos de calcio y fosfato en la superficie de las lentes acrílicas hidrofílicas en un breve periodo tras el tratamiento quirúrgico[17,18]. Las lentes de silicona también aceleran la formación de depósitos de calcio y suelen asociarse a un mayor riesgo de fimosis capsular posterior.[19]. No se recomienda la implantación de lentes multifocales en niños, ya que requieren una biometría precisa y un centrado perfecto, que pueden cambiar durante el periodo de cicatrización, debido a la posible fibrosis y al crecimiento del ojo. En los últimos años, se han publicado varios estudios en los que los autores describen el uso de LIO soportadas en el iris en niños. Sminia et al. implantaron la lente Artisan en 10 niños con una edad media de 7,4 años en los años 1991-1999. La densidad media de células endoteliales corneales (DCE) era de 2.702 células/mm² 12 años después del tratamiento quirúrgico, y era comparable a la DCE media normal para ese grupo de edad, según se recoge en la literatura.[20].
Dificultades de la cirugía de cataratas en niños
La cirugía de cataratas en niños es técnicamente más compleja que en adultos. Esto se debe a la anatomía del ojo del niño. El cristalino es pequeño, la cámara anterior es poco profunda, la cápsula anterior es muy elástica y gruesa, y la cápsula posterior es de 3 a 5 veces más fina y menos elástica que en los adultos. Además, la escasa rigidez escleral dificulta las incisiones autosellantes. Las dificultades para la midriasis requieren a menudo el uso de retractores del iris. Durante el tratamiento quirúrgico, suele observarse un aumento de la presión vítrea, normalmente como consecuencia del hundimiento escleral, lo que provoca una reducción de la profundidad de la cámara anterior y el prolapso del iris. Debido al aumento de la presión vítrea, la LIO tiende a "distorsionarse" fuera del saco capsular, en lugar de permanecer alojada en él.
Además, las complicaciones postoperatorias, tanto precoces como tardías, son más frecuentes que en los adultos. Las reacciones inflamatorias muy intensas, la fibrosis y la rápida opacificación de la cápsula posterior requieren un tratamiento intra y postoperatorio especial.
Técnica quirúrgica
Los problemas quirúrgicos más frecuentes en la cirugía pediátrica de la catarata son el manejo de la cápsula anterior y posterior, y la realización de una vitrectomía anterior. El acceso quirúrgico suele realizarse a través de la córnea o la pars plana. La amplitud media en pars plana varía de 1,5 - 2 mm en lactantes, a 3 mm a los 6 meses de edad.
La capsulorrexis manual curvilínea anterior continua, con un margen lo más liso posible, es la regla de oro para un resultado satisfactorio en la cirugía pediátrica de cataratas. Es la opción preferida de los cirujanos para los pacientes de dos años o más. Los cirujanos prefieren la vitrectomía durante los dos primeros años de vida. La capsulotomía anterior puede realizarse mediante endodiatermia por radiofrecuencia, pero el tamaño final será mayor.
La opacificación de la cápsula posterior (OCP) es el resultado de la proliferación, migración y metaplasia de células epiteliales de la región ecuatorial de la cápsula anterior a la cápsula posterior. Cuando la cápsula posterior se deja intacta durante la cirugía, la incidencia de OCP es de 100%. La aparición de la OCP suele aumentar 18 meses después de la cirugía. Por lo tanto, en niños menores de 8 años, la capsulotomía posterior debe realizarse con una vitrectomía anterior adicional.[21]. Wilson deja la cápsula posterior intacta en niños mayores de 6 años. En niños pequeños realiza una capsulotomía posterior por vía pars plana: en lactantes a 0,5 mm posterior al limbo, menores de un año a - 2 mm posterior al limbo, menores de 4 años a - 2,5 mm posterior al limbo....[3].
Cuando el cuerpo vítreo se corta por la parte posterior, hay menos riesgo de desprendimiento de retina y de edema macular cistoide.
El tratamiento de la cápsula posterior en niños con catarata congénita, recomendado por Vasavada, se describe en la Tabla II.[24].
Complicaciones tras la cirugía
La complicación más frecuente tras la cirugía de cataratas congénitas es el glaucoma secundario. Su prevalencia es de 15,4 - 19,5% en los 10 años siguientes a la cirugía.[1,2]. Por lo tanto, es muy importante someterse a revisiones médicas periódicas durante muchos años después de la intervención.
Una edad inferior a 9 meses en el momento de la cirugía y una microcórnea predisponen al desarrollo de glaucoma secundario[2]. En los niños operados antes de los 9 meses, el glaucoma es 3,8 veces más frecuente que en los niños operados después de esta edad.[2,23]. PHPV (vítreo primario hiperplásico persistente), una capsulotomía posterior primaria o una vitrectomía no predisponen al desarrollo de glaucoma secundario.[2]. En los pacientes con glaucoma, las cataratas bilaterales eran ligeramente más frecuentes que las opacidades unilaterales del cristalino.[2]. El intervalo de tiempo medio para la aparición de glaucoma tras la cirugía de una catarata congénita osciló entre unas pocas semanas y muchos años.[2,8,23].
Raramente se ha descrito desprendimiento de retina en niños tras cirugía de cataratas congénitas.[13]. La complicación postoperatoria menos frecuente es la uveítis fibrinosa.[4].
En la literatura se pueden leer informes de aumento de la miopía en niños, especialmente en los dos primeros años tras la cirugía[12,14].
En resumen
El éxito en el tratamiento de la catarata congénita depende ante todo de un diagnóstico precoz de la enfermedad. El éxito del tratamiento está ligado a la elección del momento quirúrgico óptimo, la rehabilitación visual precoz y una buena cooperación con los padres. La consecución de todas estas condiciones permite garantizar una agudeza visual adecuada, de la que dependerá la función visual en la edad adulta.
Alina Bakunowicz-?azarczyk, Beata Urban, Anna Bryl
Departamento de Oftalmología Pediátrica MU en Bialystok, Polonia
Si tiene alguna pregunta, envíe un correo electrónico: alina.lazarczyk@umb.edu.pl
CONTROVERSIAS EN EL TRATAMIENTO DE LA CATARATA PEDIÁTRICA
(texto original en inglés)
La catarata congénita puede causar discapacidad visual en los niños[1]. Constituye aproximadamente el 10% de los casos de ceguera infantil en el mundo.[2]. En particular, una gran proporción de casos se produce en países en desarrollo[3,4]. Debido al rápido desarrollo de la visión en los primeros 4 meses de vida (desarrollo del reflejo de fijación), la falta o limitación de las sensaciones visuales por el cristalino opaco suele provocar ambliopía, estrabismo, nistagmo o incluso una reducción secundaria de las neuronas de los cuerpos geniculados laterales y del córtex visual (VDS - Visual Deprivation Syndrome).
Las causas de la catarata congénita son múltiples; destacan los factores genéticos, las infecciones intrauterinas, los fármacos utilizados durante el embarazo y los trastornos metabólicos infantiles[1]. El procedimiento depende principalmente de la naturaleza y gravedad de la catarata. La ambliopía, las dificultades intra y postoperatorias y las frecuentes visitas médicas hacen que el tratamiento de la catarata congénita sea todo un reto. Todos estos dilemas hacen que la cirugía de cataratas en niños sea técnicamente más difícil que en adultos.
Indicacionescirugía de cataratas en niños
La principal indicación para la extirpación de cataratas es la nubosidad del cristalino que impide el desarrollo visual normal.
¿Cuándo operar cataratas en niños?
Se cree que la mayor disminución de la agudeza visual se produce en las primeras semanas de vida. Hasta las 14 semanas de edad, cada tres semanas de retraso en el tratamiento provoca una disminución de la agudeza visual de una línea en la tabla de Snellen. Entre las 14 y las 31 semanas de edad se produce un ligero descenso adicional de la agudeza visual. La cirugía de cataratas a las 4 semanas de edad reduce la incidencia de estrabismo y nistagmo.[5]. Se cree que las cataratas unilaterales deben operarse antes que las 6-8th semana, y catarata bilateral antes de la 10ª semana de edad[6,7]. Debido al riesgo de ambliopía, la cirugía debe realizarse lo antes posible. Sin embargo, en la literatura disponible se describe una mayor incidencia de glaucoma secundario, si el tratamiento se realiza demasiado pronto.[5,7,8].
Biometría y cálculo de la potencia de la lente intraocular
El importante crecimiento del ojo en los primeros años de vida del niño y las dificultades para predecir la longitud final del globo ocular son la principal causa de problemas en el cálculo de la potencia de la lente intraocular. Los cambios refractivos son el resultado del aumento de la longitud axial del globo ocular, que varía de 16,8 mm en el recién nacido a 22,6 mm en el adulto, y de un cambio en la curvatura de la córnea (51,2 D en el recién nacido; 43,5 D en el adulto) y del cristalino (34,4 D en el recién nacido; 18,8 D en el adulto).
Esto hace que la mayoría de los cirujanos prefieran subcorregir a los niños pequeños en el momento de la cirugía (buscando una corrección hipermetrópica) en previsión de un cambio significativo de la miopía con el tiempo. Enyedi et al presentaron directrices para las refracciones objetivo para distintas edades basadas en los resultados de su estudio. Se muestran en la tabla I[9].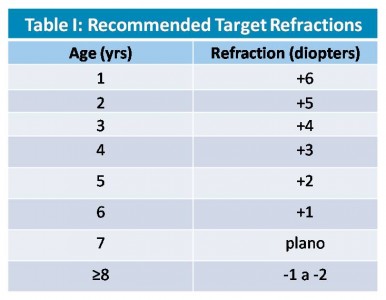
Muchos estudios no han demostrado una mayor eficacia de una de las fórmulas utilizadas en el cálculo de lentes intraoculares en niños. Normalmente se utilizan SRK II, SRK/T, Hoffer Q y Holladay [10]. Dahan et al sugieren dejar en niños menores de dos años 20% hipocorrección y 10% en niños de 2-8 años[11]. Lu et al reducen la potencia del implante en 30% en niños de 6 a 12 meses. Después de la cirugía, todos los niños deben ser corregidos con gafas o lentes de contacto[12].
Elegiruna lente intraocular (LIO)
La selección de la LIO y la edad del niño durante la implantación de la LIO son controvertidas. Debe recordarse que cuanto menor es la edad del paciente con la lente implantada, mayor es el riesgo de reintervención debido a complicaciones.[13]. Las lentes intraoculares artificiales solían implantarse en niños mayores de 2 años (en el primer año de vida los cambios de refracción son de aproximadamente 10 D). En la bibliografía disponible, la edad mínima de los pacientes quirúrgicos con una lente intraocular es de siete días.[14]. LU et al sugieren que los implantes de lentes intraoculares son seguros en niños de entre 6 y 12 meses de edad.[12]. El lugar más popular para la implantación de la LIO es el saco capsular. Proporciona el secuestro de la LIO del tejido vascularizado. La fijación de la LIO en el surco ciliar es peor, porque la lente está en contacto con la coroides. Algunos oftalmólogos pediátricos reconocen que la colocación de la lente intraocular en la bolsa para ojos afáquicos es ideal, pero es una técnica muy difícil.[15].
En observaciones anteriores se obtuvieron muy buenos resultados cuando se implantaron las lentes acrílicas hidrófobas[3,16]. La AAPOS (Asociación Americana de Oftalmología Pediátrica y Estrabismo) recomienda la lente AcrySof de una sola pieza para implantar en niños. Es fácil de implantar y es segura incluso en lactantes y en niños con microftalmia. La implantación de lentes acrílicas hidrofóbicas también se asocia a un menor riesgo de opacificación de la cápsula posterior y glaucoma secundario.[3]. En las superficies de las lentes acrílicas hidrófilas se observaron depósitos de calcio y fosfato en un corto período tras la cirugía.[17,18]. Las lentes de silicona también aceleran el desarrollo de depósitos de calcio y suelen asociarse a un mayor riesgo de fimosis capsular posterior.[19]. Las lentes multifocales, debido a la necesidad de una biometría precisa y un centrado perfecto, que pueden cambiar durante la cicatrización, la fibrosis y el crecimiento del ojo, no se recomiendan para su implantación en niños. En los últimos años, existen publicaciones en las que los autores describen el uso de LIOs en garra de iris en niños. Sminia et al implantaron lentes Artisan en 10 niños con una edad media de 7,4 años en los años 1991-1999. La densidad media de células endoteliales corneales (DCE) fue de 2702 células/mm² 12 años después de la cirugía, y era comparable a la DCE media normal para este grupo de edad descrita en la literatura.[20].
Dificultades durante la cirugía de cataratas en niños
La cirugía de cataratas en niños es técnicamente más difícil que en adultos. Esto se debe a la anatomía del ojo infantil. El cristalino es pequeño, la cámara anterior es poco profunda, la cápsula anterior es muy elástica y gruesa, la cápsula posterior es de 3 a 5 veces más fina y menos elástica que en los adultos. Además, la baja rigidez escleral dificulta la incisión autosellante. Las dificultades con la midriasis requieren a menudo el uso de retractores del iris. Durante la intervención quirúrgica suele observarse un aumento de la presión vítrea, normalmente como consecuencia del hundimiento escleral, lo que da lugar a una menor profundidad de la cámara anterior y al prolapso del iris. Debido al aumento de la presión vítrea, la LIO tiende a "retorcerse" del saco capsular, en lugar de colocarse dentro de él. Además, las complicaciones postoperatorias tempranas y tardías son más frecuentes que en los adultos. Las reacciones inflamatorias muy fuertes, la fibrosis y la rápida opacificación de la cápsula posterior requieren un tratamiento intra y postoperatorio especial.
Técnica quirúrgica
Los dilemas operativos más frecuentes en la cirugía pediátrica de la catarata son: el manejo con cápsula anterior y posterior, y la realización de vitrectomía anterior. El acceso quirúrgico se realiza generalmente a través de la córnea o de la pars plana. La anchura media de la pars plana oscila entre 1,5-2 mm en el recién nacido, y 3 mm a los 6 meses de edad. La capsulorrexis curvilínea anterior continua manual (ACCC) con el borde más regular es el patrón oro para el éxito de la cirugía pediátrica de la catarata. Los cirujanos la prefieren para pacientes a partir de 2 años. Los cirujanos prefieren la vitrectorrexis durante los 2 primeros años de vida. La capsulotomía anterior puede realizarse mediante endodiatermia por radiofrecuencia, pero el tamaño final será mayor. La opacificación de la cápsula posterior (OCP) es el resultado de la proliferación, migración y metaplasia de células epiteliales que derivan de la región ecuatorial de la cápsula anterior a la cápsula posterior. Cuando la cápsula posterior se deja intacta durante la cirugía, la incidencia de OCP es de 100%,. La incidencia de OCP suele aumentar 18 meses después de la cirugía. Por lo tanto, en niños menores de 8 años la capsulotomía posterior debe realizarse con una vitrectomía anterior adicional.[21]. Wilson deja la cápsula posterior intacta en niños mayores de 6 años. En niños pequeños realiza la capsulotomía posterior a través de la pars plana: en lactantes 0,5 mm posterior al limbo, menores de 1 año - 2 mm posterior al limbo, menores de 4 años - 2,5 mm posterior al limbo y en niños mayores de 4 años - 3 mm posterior al limbo.[3]. Cuando el cuerpo vítreo se corta por la parte posterior, se asocia a un menor riesgo de desprendimiento de retina y de edema macular cistoide. El manejo de la cápsula posterior en niños con catarata congénita, recomendado por Vasavada, se muestra en la Tabla II[22].

Complicaciones después de la cirugía
La complicación más frecuente descrita tras la cirugía de la catarata congénita es el glaucoma secundario. Su prevalencia se determina en 15,4 -19,5% a los 10 años de la cirugía.[1,2]. Por lo tanto, los exámenes médicos periódicos durante muchos años después de la cirugía son muy importantes. La edad inferior a nueve meses en el momento de la intervención y la microcórnea predisponen al desarrollo de glaucoma secundario.[2]. En los niños operados antes de los 9 meses de edad, el glaucoma se produce 3,8 veces más a menudo que en los niños operados después de este periodo de la vida[2,23]. PHPV, capsulotomía posterior primaria o vitrectomía anterior no predisponen al desarrollo de glaucoma secundario[2]. En los pacientes con glaucoma, la catarata bilateral era ligeramente más frecuente que las opacidades unilaterales del cristalino.[2]. El tiempo medio transcurrido hasta el glaucoma tras la cirugía de cataratas congénitas osciló entre semanas y muchos años.[2,8,23]Se han descrito casos raros de desprendimiento de retina en niños tras cirugía de cataratas congénitas.[13]. La complicación postoperatoria menos frecuente es la uveítis fibrinosa[4].
En la literatura disponible se pueden encontrar informes de aumento de la miopía en niños, especialmente en los 2 primeros años tras la cirugía[12,14].
Resumen
El éxito en el tratamiento de la catarata congénita depende principalmente del diagnóstico precoz de la enfermedad. El éxito influye en el momento óptimo de la cirugía, la rehabilitación visual precoz y la buena cooperación con los padres. El cumplimiento de todos estos criterios determina una agudeza visual útil, de la que dependerá el funcionamiento en la edad adulta.
Alina Bakunowicz-?azarczyk, Beata Urban, Anna Bryl
Departamento de Oftalmología Pediátrica MU en Bialystok, Polonia
Para cualquier pregunta, envíe un correo electrónico: alina.lazarczyk@umb.edu.pl
Referencias
1. Chan WH, Biswas S, Ashworth JL, Lloyd IC. Catarata congénita e infantil: etiología y tratamiento. Eur J Pediatr. 2012 Abr;171(4):625-30.
2. Swamy BN, Billson F, Martin F, Donaldson C, Hing S, Jamieson R, Grigg J, Smith JE. Glaucoma secundario tras cirugía pediátrica de cataratas. Br J Ophthalmol. 2007 Dic;91(12):1627-30.3. Wilson ME, Pandey SK, Thakur J. Paediatric cataract blindness in the developing world: surgical techniques and intraocular lenses in the new millennium. Br J Ophthalmol 2003;87:14-19
4. Khanna RC, Foster A, Krishnaiah S, Mehta MK, Gogate PM. Visual outcomes of bilateral congenital and developmental cataracts in young children in south India and causes of poor outcome. Indian J Ophthalmol. 2013 Feb;61(2):65-70.
5. Abedul EE, Cheng C, Stager DR Jr, Weakley DR Jr, Stager DR Sr. Periodo crítico para el tratamiento quirúrgico de las cataratas bilaterales congénitas densas. 2009 J AAPOS. 2009 feb;13(1):67-71.
6. Lagrèze WA. El tratamiento de la catarata en la infancia 2009 Klin Monbl Augenheilkd. 2009 Ene;226(1):15-21.
7. Lloyd IC, Ashworth J, Biswas S, Abadi RV. Avances en el tratamiento de la catarata congénita e infantil. Eye (Lond). 2007 Oct;21(10):1301-9.
8. Lambert SR, Purohit A, Superak HM, Lynn MJ, Beck AD. Riesgo a largo plazo de glaucoma tras cirugía de cataratas congénitas. Am J Ophthalmol. 2013 Apr 30. pii: S0002-9394(13)00177-3.
9. Enyedi LB, Peterseim MW, Freedman SF, Buckley EG. Cambios refractivos tras la implantación de lentes intraoculares pediátricas. Am J Ophthalmol. 1998 Dic;126(6):772-81.
10. Andreo LK, Wilson ME, Saunders RA. Valor predictivo de las fórmulas de regresión y teóricas de LIO en la implantación de lentes intraoculares pediátricas. J Pediatr Ophthalmol Strabismus. 1997 Jul-Ago;34(4):240-3.
11. Dahan E, Drusedau MU. Elección de la lente y potencia dióptrica en la pseudofaquia pediátrica. J Cataract Refract Surg. 1997;23 Suppl 1:618-23.
12. Lu Y, Ji YH, Luo Y, Jiang YX, Wang M, Chen X Graefes Resultados visuales y complicaciones de la implantación primaria de lentes intraoculares en lactantes de 6 a 12 meses. Arch Clin Exp Ophthalmol. 2010 mayo;248(5):681-6.
13. Keech RV, Lengua AC, Scott WE. Complicaciones tras la cirugía de cataratas congénitas e infantiles. Am J Ophthalmol. 1989 Ago 15;108(2):136-41.
14. O'Keefe M, Fenton S, Lanigan B. Resultados visuales y complicaciones de la implantación de lentes intraoculares de cámara posterior en el primer año de vida. J Cataract Refract Surg. 2001 dic;27(12):2006-11.
15. Peterseim MW, Wilson ME. Implantación de lentes intraoculares bilaterales en la población pediátrica. Oftalmología. 2000 Jul;107(7):1261-6.
16. Knight-Nanan D, O'Keefe M, Bowell R. Resultados y complicaciones de las lentes intraoculares en niños con cataratas. J Cataract Refract Surg. 1996 Jul-Ago;22(6):730-6.
17. Luo L, Lin H, Chen W, Wang C, Zhang X, Tang X, Liu J, Congdon N, Chen J, Lin Z, Liu Y: In-the-bag intraocular lens placement via secondary capsulorhexis with radiofrequency diathermy in pediatric aphakic eyes. PLoS One. 2013 Abr 24;8(4):e62381
18. Vasavada AR, Raj SM, Shah A, Shah G, Vasavada V, Vasavada V. Comparación de la opacificación de la cápsula posterior con lentes intraoculares acrílicas hidrofóbicas y acrílicas hidrofílicas. J Cataract Refract Surg. 2011 Jun;37(6):1050-9.
19. Pehere NK, Bojja S, Vemuganti GK, Vaddavalli PK, Samant M, Jalali S, Bhate M. Opacificación de lentes intraoculares implantadas durante la infancia: estudio clinicopatológico de 4 lentes intraoculares explantadas.. Ophthalmology. 2011 Nov;118(11):2128-2132.
20. Kleinmann G, Mamalis N, Apple DJ, Hesse EI. Opacificación de la lente intraocular acrílica hidrofílica Acryl C160. J Cataract Refract 2006 Feb;32(2):367-8.
21. Dorey MW, Brownstein S, Colina VE, Mateo B, Botton G, Kertes PJ, El-Defrawy S. Patogénesis propuesta para la opacificación postoperatoria retardada de la lente intraocular de hidrogel Hydroview. Am J Ophthalmol. 2003 mayo;135(5):591-8.
22. Sminia ML, Odenthal MT, Prick LJ, Diputado Mourits, Völker-Dieben HJ. Seguimiento a largo plazo del endotelio corneal tras la implantación de una LIO afáquica fijada al iris para la catarata bilateral en niños. J Cataract Refract Surg. 2011 mayo;37(5):866-72.
23. Dahan E, Salmenson BD. Pseudophakia in children: precautions, technique, and feasibility. J Cataract Refract Surg. 1990 Ene;16(1):75-82.
24. Vasavada AR, Praveen MR, Tassignon MJ, Shah SK, Vasavada VA, Van Looveren J, De Veuster I, Trivedi RH. Manejo de la cápsula posterior en la cirugía de la catarata congénita. J Cataract Refract Surg 2011 J Cataract Refract Surg. 2011.
25. B. Urban, A. Bakunowicz-?azarczyk: Glaucoma afáquico tras cirugía pediátrica de cataratas con y sin implantación de lente intraocular. Klin. Oczna 2010,112(4-6):105-107.
Dr. Carmelo Chines
Director responsable
